に対するイムデトラの有効性
及び 安全性 が報告され、
電子添文が改訂されました
ガイドラインにおけるイムデトラの位置づけ
肺癌診療ガイドライン―胸膜中皮腫・胸腺腫瘍含む―2025年版
二次治療以降にタルラタマブ療法を行うよう強く推奨する。
〔推奨の強さ:1,エビデンスの強さ:B〕
-
解説
プラチナ製剤併用療法を含む2レジメン以上の治療歴を有するPS 0-1の再発小細胞肺癌を対象に,タルラタマブの第Ⅱ相試験が行われた(Dellphi-301試験)1)。タルラタマブ10mg群のORRは40%,PFS中央値は4.9カ月,OS中央値は14.3カ月であった。有害事象について,全グレードのCRSの頻度は51%,ICANSに関する神経学的有害事象の頻度は8%,グレード3以上の全治療関連有害事象は26%に認められた。
その後,プラチナ製剤併用療法後に増悪したPS 0-1の再発小細胞肺癌を対象に,タルラタマブと細胞傷害性抗癌薬単剤療法(AMR,NGT,またはlurbinectedin)を比較する第Ⅲ相試験が行われた(DeLLphi-304試験)2)。細胞傷害性抗癌薬単剤療法群に対するタルラタマブ群のOSはHR 0.60(95%CI 0.47-0.77,P<0.001,中央値:13.6カ月 vs 8.3カ月)であり,タルラタマブ群は細胞傷害性抗癌薬単剤療法群に対して,主要評価項目であるOSを有意に延長した。層別化因子の1つであるプラチナ製剤併用療法終了からの期間は,90日未満が全体の44%,90日以上180日未満が32%,180日以上が24%で,OSのHRはサブグループ間で同等であった。タルラタマブ群は細胞傷害性抗癌薬単剤療法群に対して,副次評価項目であるPFSも有意に延長した(HR 0.71,95%CI 0.59-0.86,P=0.002,中央値:5.3カ月 vs 4.3カ月)。ORRもタルラタマブ群が高かった(35% vs 20%)。グレード3以上の全治療関連有害事象はタルラタマブ群27%,細胞傷害性抗癌薬単剤療法群62%であった。タルラタマブ群の全グレードのCRSの頻度は56%,ICANSの頻度は6%であった。
タルラタマブに特徴的な有害事象として,発熱,頻呼吸,頭痛,頻脈,低血圧,皮疹,低酸素血症などの症状を呈するCRSや,振戦,昏迷,興奮,けいれん,失語などを呈するICANSが報告されており,それぞれに対して適切な管理が必要となる。本剤の投与に際しては,添付文書や適正使用ガイドなどを参考に,厳密な副作用モニタリングと管理ができる医療環境のもとで治療を行うことが望ましい。
以上より,PS 0-1の再発小細胞肺癌に対して,二次治療以降にタルラタマブ療法を行うよう勧められる。エビデンスの強さはB,また総合的評価では行うよう強く推奨(1で推奨)できると判断した。下記に,推奨度決定のために行われた投票結果を記載する。
投票者の所属委員会:薬物療法及び集学的治療小委員会(薬剤師2名,看護師2名,患者1名を含む)/実施年度:2025年
行うことを強く推奨 行うことを弱く推奨 推奨に至る根拠が
明確ではない行わないことを
弱く推奨行わないことを
強く推奨87%(26/30) 13%(4/30) 0% 0% 0% 1)Ahn MJ, Cho BC, Felip E, et al. Tarlatamab for patients with previously treated small-cell lung cancer. N Engl J Med. 2023;389(22):2063-75.
2)Mountzios G, Sun L, Cho BC, et al. Tarlatamab in small-cell lung cancer after platinum-based chemotherapy. N Engl J Med. 2025;393(4):349-61. Epub 2025 Jun 2.本著作物は日本肺癌学会が作成したものであり、本著作物の内容に関する質問、問い合わせ等は日本肺癌学会にご連絡ください。アムジェン株式会社は、日本肺癌学会及び発行元である金原出版から許諾を得て、本著作物を内容の改変を行うことなく転載し、使用しています。日本肺癌学会編:肺癌診療ガイドライン2025年版.Ⅲ-4.再発小細胞肺癌.金原出版https://www.haigan.gr.jp/publication/guideline/examination/2025/1/3/250103040100.html#cq17(アクセス日:2025年11月10日)
イムデトラ群でOSが有意に延長
国際共同第Ⅲ相試験臨床成績 (20210004試験、DeLLphi-304試験)1,2)
OS中央値はイムデトラ群13.6ヵ月(95%CI:11.1, 推定不能)、標準治療群8.3ヵ月(95%CI:7.0, 10.2)でした。イムデトラ群の標準治療群に対するHRは0.599(95%CI:0.468, 0.768)、p<0.001[層別log-rank検定、有意水準(片側)0.0103]であり、イムデトラ群においてOSが有意に延長されることが検証されました。
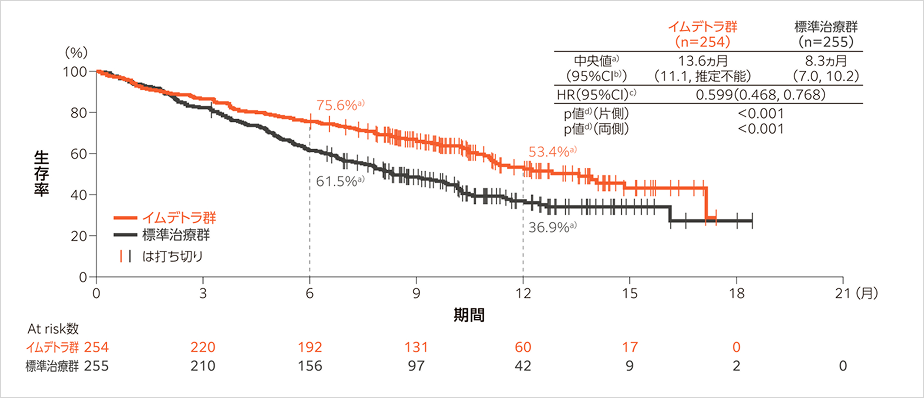
a)Kaplan-Meier法、b)Brookmeyer-Crowley法、c)層別Cox比例ハザードモデル、d)層別log-rank検定
層別因子:抗PD-1又は抗PD-L1による治療歴(有、無)、化学療法未治療期間(180日以上、90日以上かつ180日未満、90日未満)、脳転移(有、無)又は標準治療(アムルビシン/Topotecan、Lurbinectedin)
データカットオフ日:2025年1月29日、フォローアップ期間中央値:イムデトラ群11.2ヵ月 標準治療群11.7ヵ月
-
安全性1)
有害事象一覧(いずれかの群で20%以上の有害事象)(安全性解析対象集団)
例数 イムデトラ群
(n=252)標準治療群
(n=244)サイトカイン放出症候群 142(56.3) 3(1.2) 食欲減退 89(35.3) 54(22.1) 貧血 78(31.0) 156(63.9) 疲労 72(28.6) 74(30.3) 便秘 72(28.6) 54(22.1) 発熱 69(27.4) 27(11.1) 例数 イムデトラ群
(n=252)標準治療群
(n=244)悪心 61(24.2) 78(32.0) 味覚不全 61(24.2) 4(1.6) 好中球減少症 27(10.7) 76(31.1) 白血球減少症 24(9.5) 54(22.1) 血小板減少症 14(5.6) 62(25.4) - 重篤な有害事象はイムデトラ群で129例(51.2%)、標準治療群で125例(51.2%)に認められた。主な事象(5例以上)は、イムデトラ群でサイトカイン放出症候群43例(17.1%)、発熱14例(5.6%)、肺炎10例(4.0%)、免疫エフェクター細胞関連神経毒性症候群9例(3.6%)、呼吸困難6例(2.4%)、発熱性好中球減少症、敗血症及び低ナトリウム血症各5例(2.0%)、標準治療群で発熱性好中球減少症24例(9.8%)、肺炎21例(8.6%)、血小板減少症11例(4.5%)、貧血10例(4.1%)、好中球減少症及び血小板数減少各6例(2.5%)、汎血球減少症5例(2.0%)であった。
- 投与中止に至った有害事象はイムデトラ群で13例(5.2%)、標準治療群で30例(12.3%)に認められた。主な事象(2例以上)は、イムデトラ群で肺炎3例(1.2%)、標準治療群で貧血及び心停止各3例(1.2%)、血小板減少症、肺炎、気道感染及び呼吸不全各2例(0.8%)であった。
- 死亡に至った有害事象はイムデトラ群で20例(7.9%)、標準治療群で21例(8.6%)に認められた。主な事象(2例以上)は、イムデトラ群で肺炎4例(1.6%)、心肺停止3例(1.2%)、敗血症2例(0.8%)、標準治療群で肺炎6例(2.5%)、心停止3例(1.2%)、呼吸不全2例(0.8%)であった。なお、治験薬との因果関係が認められた死亡に至った副作用は、イムデトラ群では免疫エフェクター細胞関連神経毒性症候群1例(0.4%)※であった。
※:当該死亡例は、持続する発熱、低酸素血症、低血圧に加え、進行性の神経学的低下を呈していたことから、ICANSに起因するものと考えられた。
治験薬との因果関係が否定できない有害事象を副作用とし、有害事象名はMedDRA ver.27.1を用いてコード化した。CRS及びICANSのGrade分類はASTCTコンセンサス(2019年)に準じた。その他のGrade分類はCTCAE ver.5.0に準じた。
データカットオフ日:2025年1月29日 -
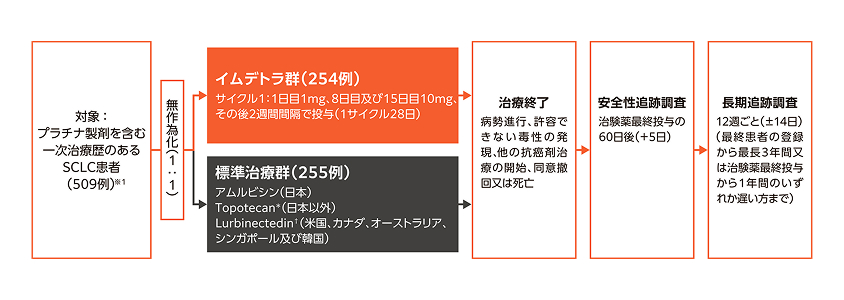
試験概要1,2)目的:
白金系抗悪性腫瘍剤を含む1つの化学療法治療歴のある小細胞肺癌患者を対象に、イムデトラの標準治療に対する有効性、安全性を評価する
対象:白金系抗悪性腫瘍剤を含む1つの化学療法治療歴のある小細胞肺癌患者509例(日本人35例含む)
試験デザイン:国際共同第Ⅲ相、無作為化、非盲検、多施設
層別因子:抗PD-1又は抗PD-L1による治療歴(有、無)、化学療法未治療期間(180日以上、90日以上かつ180日未満、90日未満)、脳転移(有、無)又は標準治療(アムルビシン/Topotecan、Lurbinectedin)
*: 和名ノギテカン †:本邦未承認※1: 試験に組み入れられた509例のうち13例(イムデトラ群2例、標準治療群11例)は治験薬の投与を1回も受けなかったが、解析に含められた。投与方法:- イムデトラ:
イムデトラ1mgをサイクル1の1日目に、10mgをサイクル1の8日目及び15日目、その後2週間間隔で投与する。 - アムルビシン※2:
〔日本〕アムルビシン40mg/m2を1日目から3日目まで3週間間隔で投与する。 - Topotecan※3:
〔日本と中国以外〕Topotecan1.5mg/m2又は2.3mg/m2を1日目から5日目まで3週間間隔で投与する。 〔中国〕Topotecan1.2mg/m2又は2.3mg/m2を1日目から5日目まで3週間間隔で投与する。 - Lurbinectedin:
〔米国、カナダ、オーストラリア、シンガポール及び韓国〕Lurbinectedin3.2mg/m2を1日目に3週間間隔で投与する。
※2:本邦におけるアムルビシンの用法及び用量は「通常、成人にはアムルビシン塩酸塩として45mg(力価)/m2(体表面積)を約20mLの日局生理食塩液あるいは5%ブドウ糖注射液に溶解し、1日1回3日間連日静脈内に投与し、3〜4週間休薬する。これを1クールとし、投与を繰り返す。なお、患者の状態により適宜減量する。」である。
※3:本邦におけるノギテカンの用法及び用量は「ノギテカンとして、通常、成人に1日1回、1.0mg/m2(体表面積)を5日間連日点滴静注し、少なくとも16日間休薬する。これを1コースとして、投与を繰り返す。なお、患者の状態により適宜増減する。」である。主要評価項目:全生存期間(OS)(検証的解析項目)
重要な副次評価項目:無増悪生存期間(PFS)[治験担当医師判定]、患者報告アウトカム(PRO)
副次評価項目:客観的奏効率(ORR)[治験担当医師判定]、奏効期間(DOR)[治験担当医師判定]、安全性、忍容性、薬物動態、免疫原性など
研究の限界:非盲検であったことに加え、適格基準がEastern Cooperative Oncology Group(ECOG) PS 0又は1に限定されていた点や黒人患者の登録数が少ない点が、患者集団の代表性に制限を与えた可能性がある。
解析計画:【対象集団】有効性解析対象集団は、無作為化された全患者であるintention-to-treat解析対象集団(ITT解析対象集団)とした。安全性解析対象集団は、治験薬を少なくとも1回投与された全患者とした。
【主要評価項目】本試験はOSの中間解析を1回、主要解析を1回実施する群逐次デザインであった。全体のαを両側0.05としたlog-rank検定を行った場合、両群で合計345件のOSイベントにより、HRが0.7の仮定の下で91%の検出力でイムデトラの優越性が示される。中間解析は約259件のOSイベントが発生した時点で実施することとしていた。中間解析及び主要解析時の境界値は、O’Brien-Fleming法によるLan-DeMetsのα消費関数を用いて調整した。
OS中央値に関してKaplan-Meier推定値及び95%CIを二重対数変換によるBrookmeyer-Crowley法(1982)を用いて要約した。HR及び95%CIは層別Cox比例ハザードモデルを用いて推定し、群間比較には層別log-rank検定を用いた。特定の時点(例:6ヵ月、12ヵ月、18ヵ月時点)のOS率はKaplan-Meier法により推定した。【層別因子】層別因子は、抗PD-1又は抗PD-L1による治療歴(有、無)、化学療法未治療期間(180日以上、90日以上かつ180日未満、90日未満)、脳転移(有、無)又は標準治療(アムルビシン/Topotecan、Lurbinectedin)とされた。過剰な層別を防ぐため層別因子を化学療法未治療期間(90日以上、90日未満)に統合する場合もある。
【共変量】共変量は、地域(北米及び欧州、その他の地域)、直近の前治療に対する最良効果、年齢(65歳未満、65歳以上)、性別(男性、女性)、人種(白人、黒人、アジア人、その他)、ベースラインの肝転移、初診時の病期(0期、Ⅰ期、Ⅱ期、Ⅲ期、Ⅳ期、不明)、喫煙歴(なし、現在、過去)、ベースラインのECOG PS(0、1)、ベースラインのLDH値とされた。
【安全性】注目すべき有害事象としてサイトカイン放出症候群(CRS)、神経学的事象[免疫エフェクター細胞関連神経毒性症候群(ICANS)を含む]、神経関連事象、好中球減少症、過敏症の評価を行った。CRS及びICANSは米国移植細胞治療学会(ASTCT)の判定基準に基づき重症度判定し、それ以外の有害事象はCTCAE ver.5.0に基づき重症度判定した。
- イムデトラ:
-
References
- 社内資料:20210004試験 国際共同第Ⅲ相試験(DeLLphi-304試験)(TAR90039)(電子添文改訂時の評価資料)
- Mountzios G et al. N Engl J Med. 2025; 393: 349-361.(TAR00129)
[利益相反:本試験はAmgen社の支援により行われた。]