監修
愛知県がんセンター研究所
がん標的治療トランスレーショナルリサーチ分野 分野長
衣斐 寛倫 先生
はじめに
2025年9月19日に、ルマケラス®(一般名:ソトラシブ)について「がん化学療法後に増悪したKRAS G12C変異陽性の治癒切除不能な進行・再発の結腸・直腸癌」の効能又は効果が、パニツムマブとの併用において追加されました。
ルマケラス+パニツムマブ併用療法は、標準治療後の有効な治療法が確立していないKRAS G12C変異陽性の治癒切除不能な進行・再発の結腸・直腸癌における、新たな治療選択肢となることが期待されます。
今回は、KRAS G12C変異陽性大腸癌の病態と、ルマケラスとパニツムマブの併用の意義について深掘りします。
大腸癌におけるKRAS変異の頻度とKRAS変異のプロファイル
KRAS遺伝子変異は大腸癌の30%以上に認められ、膵癌に次いで高頻度に発現すると報告されています(図1)1)。KRAS変異の中でも「KRAS G12C変異」サブタイプは、大腸癌全体の約2.8%に認められます2)。-
図1 癌種別:KRAS変異の頻度(上)とKRASサブタイプの割合(下)
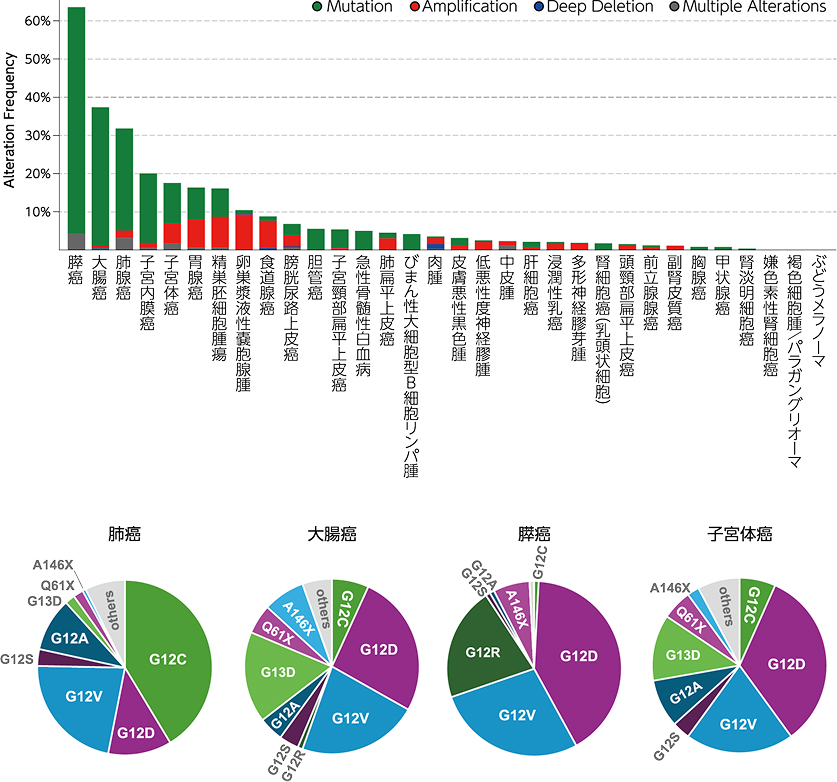
【上図】 TCGA(The Cancer Genome Atlas Program)の32癌種におけるKRAS変異の頻度。
cBioPortal(https://www.cbioportal.org)を用いて作成。【下図】肺癌、大腸癌、膵癌、子宮体癌におけるKRAS変異サブタイプの割合。
KRAS G12C変異陽性大腸癌の予後
KRAS G12C変異陽性大腸癌は、KRAS野生型や他のサブタイプのKRAS変異と比較して予後不良であり、アンメットニーズの高い疾患であると考えられています(図2、3)2)。-
図2 遺伝子変異状況別の全生存期間(OS)
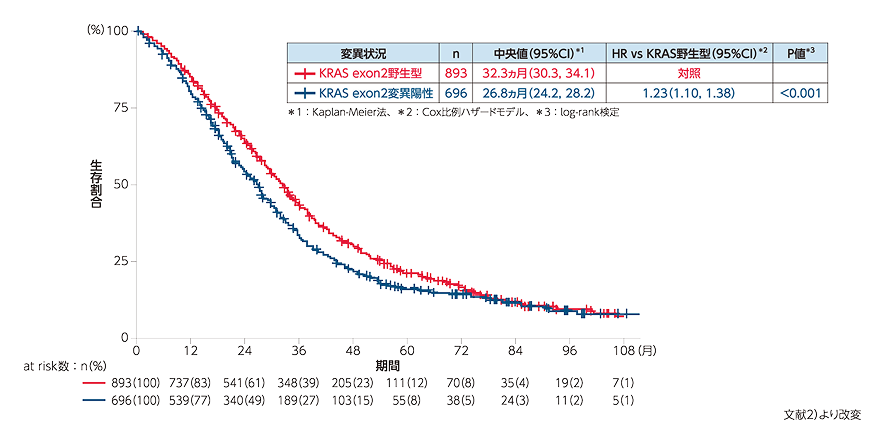
図3 全生存期間(OS):KRAS G12C変異とそれ以外のKRAS変異の比較
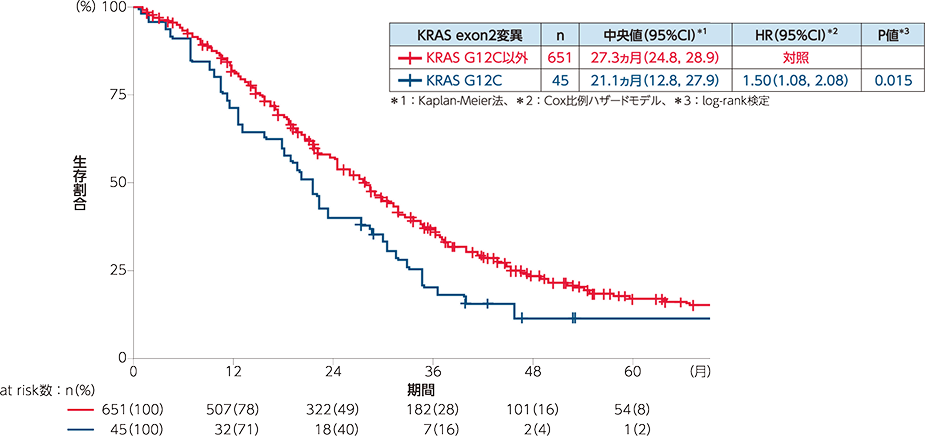
【目的】KRAS G12C変異陽性の転移を有する結腸・直腸癌の予後を、リアルワールドデータを用いて評価すること。
【試験デザイン】レトロスペクティブ研究
【対象】2005年1月~2017年12月に、日本の4つの医療施設(国立がん研究センター東病院、愛知県がんセンター、静岡県立静岡がんセンター及び北海道大学病院)において薬物治療を受けた転移を有する結腸・直腸癌の患者について追跡調査を実施した。
ECOG PS 0-2、組織学的に確認された結腸・直腸腺癌(KRAS共変異、KRAS exon3/4変異及びNRAS変異を除く)などの条件を満たした1,632例。
【方法】KRAS G12C変異陽性症例と、それ以外のKRAS変異陽性症例について生存期間を比較した。
【解析方法】OS及びPFSは、Kaplan-Meier法を用いて算出した。群間差はlog-rank法にて検定し、ハザード比はCox比例ハザードモデルを用いて推定した。
【limitations】非ランダム化レトロスペクティブ研究である。KRAS G12C変異陽性の症例数が少ない。対象がアジア人のみである。
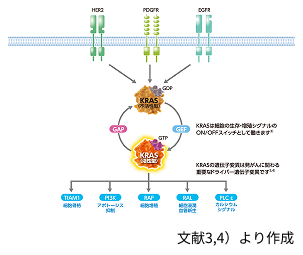
KRASの働き
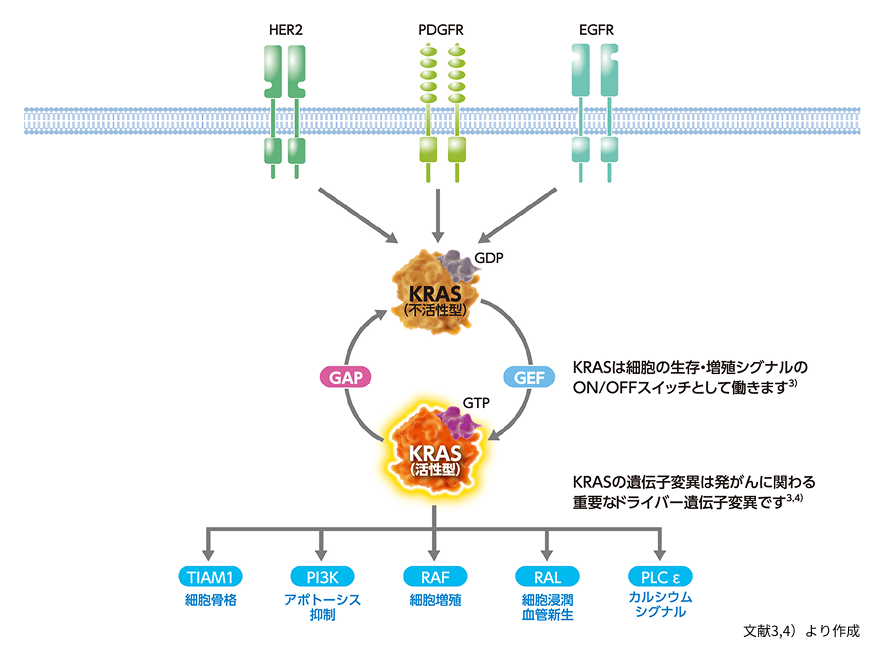
KRASは、細胞周期、細胞移動、アポトーシス、老化など様々な生体機能に関与するシグナル伝達経路の中心的な役割を担っています3,4)。KRASは低分子量GTPaseと呼ばれるタンパク質の一つで、GTPが結合した活性状態と、GDPが結合した不活性状態を切り替えることでシグナル伝達のON/OFFスイッチとして機能しています (図4)3)。なお、正常細胞では増殖していない場合は、KRASは不活性型にとどまっています。
-
図4 正常細胞におけるKRASを介したシグナル伝達
KRAS変異陽性腫瘍におけるKRAS
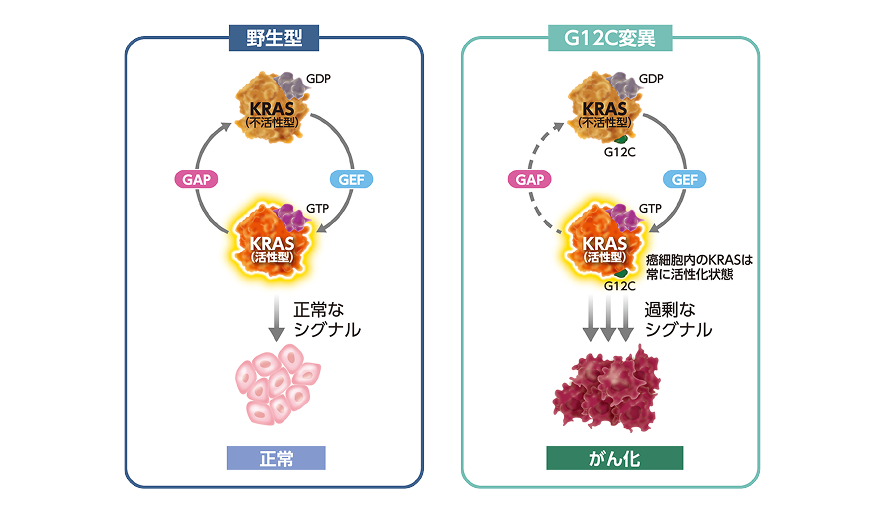
KRASが変異すると活性型のKRASが優位になります。活性化されたKRASは、様々なシグナルを継続的に下流へと伝達します。このようなKRASのON/OFFスイッチ機構の破綻が、癌の発生や進展を引き起こすと考えられます(図5)5)。-
図5 野生型KRASとKRAS G12C変異タンパクのシグナル伝達
変異型KRASではON/OFFスイッチが破綻しているため、過剰なシグナル伝達が持続します
KRAS G12C阻害剤ルマケラスの作用機序
KRAS阻害剤の開発は難航し、長い間「KRASはundruggable target」とされてきました。しかし、2013年にSwitch Ⅱポケットが発見される6)と一挙に研究開発が進み、世界初のKRAS G12C阻害剤ルマケラスの誕生に至りました。
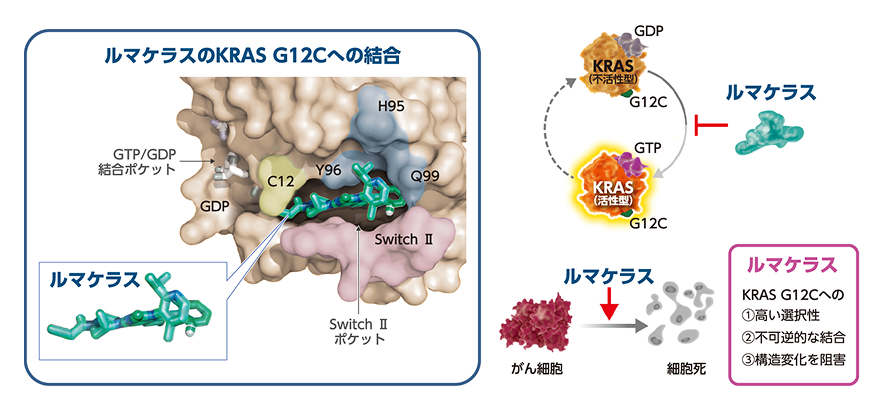
ルマケラスはSwitch Ⅱポケットの近傍にあるG12Cのシステイン残基と不可逆的に結合して、KRASタンパクの不活性型から活性型への変化を阻害します(図6)7,8)。その結果、活性型KRASの割合を減少させ、シグナル伝達をブロックして癌細胞をアポトーシスに誘導すると考えられます。
-
図6 ルマケラスの結合部位
ルマケラスはSwitch Ⅱポケットに結合し、KRASの活性型への構造変化を阻害します
KRAS阻害によるフィードバック
MAPKシグナル伝達経路ではRAS、MEK、ERKが順番に活性化し、それにより新たに合成されたタンパク質がMAPKシグナル伝達経路のタンパク質を抑制する、というフィードバック機構が働いています(図7A)。KRASやBRAFの変異によりMAPKシグナルが活性化するとフィードバックも強まり、シグナルの強度は一定の範囲に保たれるように厳密に制御されています(図7B)。
KRASを阻害した場合、その下流のシグナルが抑制されるので、フィードバックも弱まります。その結果、MAPKシグナルが再活性化されます(図7C)1)。
-
図7 MAPKのフィードバック機構と再活性化
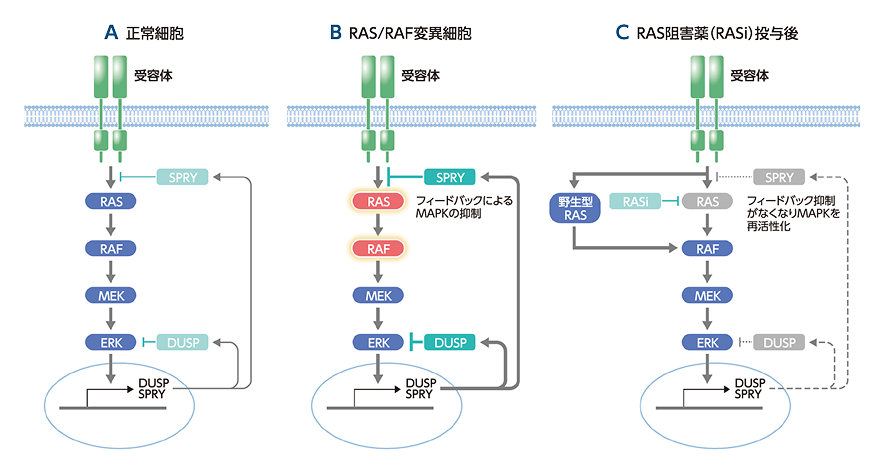
KRAS変異陽性大腸癌におけるKRAS阻害によるEGFR再活性化
肺癌や膵癌ではMAPKシグナル抑制後に複数の受容体型チロシンキナーゼ(RTK)が再活性化されるのに対し、大腸癌では主にEGFRが再活性化されることが示されています1,9,10)。KRAS変異陽性の大腸癌では、KRASを阻害するとその下流が抑制され、その結果、フィードバックが弱まり、EGFRが再活性化されます(図8)1,10)。
図8 KRAS G12C変異陽性大腸癌におけるKRAS G12C阻害によるEGFRの再活性化
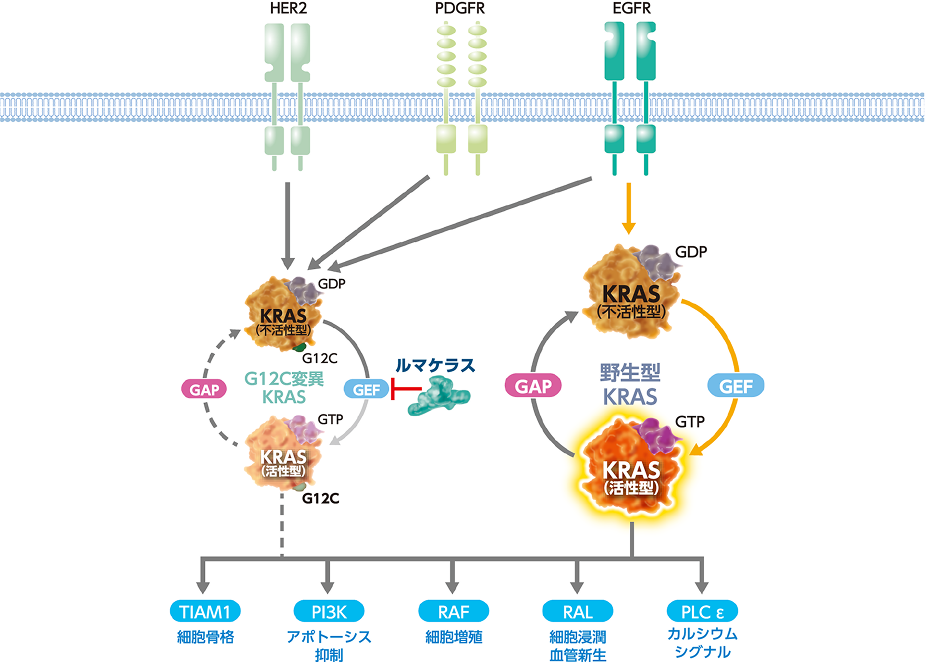
KRAS G12C変異陽性大腸癌におけるルマケラス+パニツムマブ併用の意義
大腸癌ではMAPKシグナル抑制後、主にEGFRが再活性化され、これがKRAS G12C阻害剤の一次耐性の一因とされています1,9,10)。また、大腸癌細胞株を用いた研究において、EGFRを阻害するとKRAS G12C阻害剤投与後に起きるMAPKシグナルの再活性化が抑制されることが示されています10)。
パニツムマブは、EGFRの二量体化を阻害し、PI3K及びKRAS/NRAS野生型を介したシグナル伝達を阻害して抗腫瘍効果を示します(図9)。KRAS G12Cを阻害するルマケラスとEGFRを阻害するパニツムマブの併用は、大腸癌において重要な意義があると考えられます1)。
図9 ルマケラス+パニツムマブ併用時のシグナル伝達
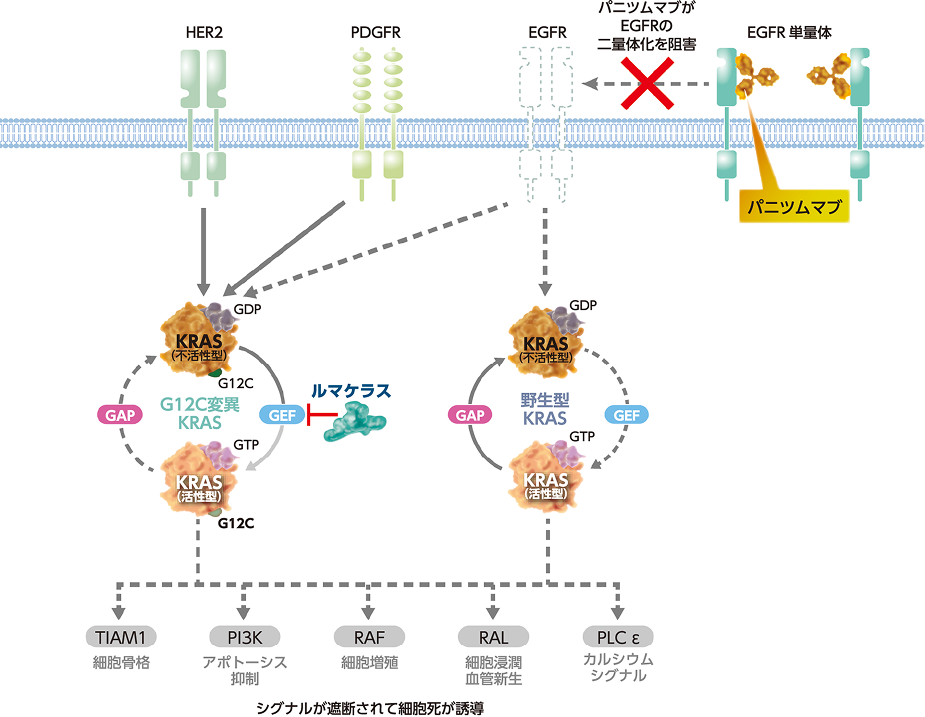
これまでRAS変異陽性大腸癌に抗EGFR薬の適応はありませんでした
RAS遺伝子変異を有する患者では抗EGFR薬(セツキシマブ、パニツムマブ)の化学療法への上乗せ効果が認められないことが示されています11,12)。そのため、抗EGFR薬はRAS遺伝子野生型のみに適応が認められていました。
図10に示すように、KRAS変異陽性の癌細胞では活性型のKRASが優位となっていて、抗EGFR薬で野生型RAS経路を阻害しても、変異型KRASが下流へシグナルを伝達してしまうと推察されます。
-
図10 KRAS変異陽性大腸癌における抗EGFR薬の作用
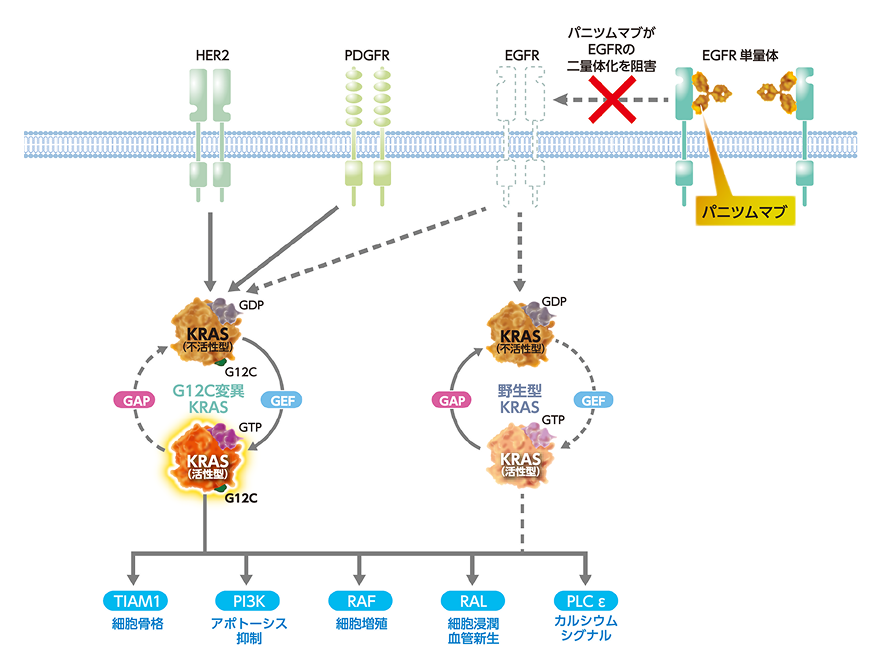
「警告・禁忌を含む注意事項等情報」等は電子化された添付文書をご参照ください。
国際共同第Ⅲ相試験(CodeBreaK 300)13,14)
試験デザイン
ルマケラス+パニツムマブ併用の意義を踏まえて、CodeBreaK 300試験が実施されました。図11にその概要を示します。
CodeBreaK 300試験には、国内の承認内容と異なる方法で治験薬が投与された患者が含まれていますが、承認時評価資料のため掲載しました。なお、ルマケラス240mg+パニツムマブ群については、安全性データのみ示します。
-
図11 CodeBreaK 300の試験デザイン
多施設共同[12ヵ国(日本、韓国、台湾、フランス、ドイツ、ギリシャ、イタリア、スペイン、英国、メキシコ、米国、オーストラリア)の67施設]、ランダム化、非盲検、実薬対照試験
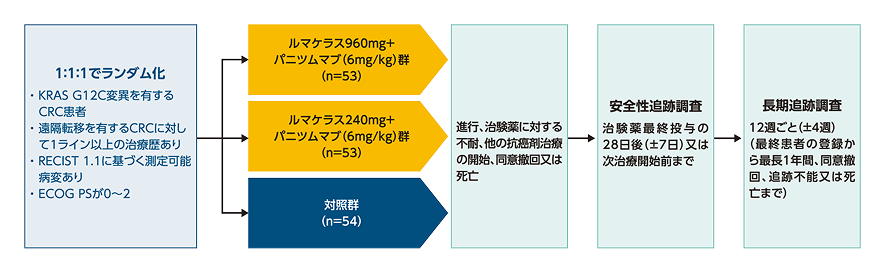
<層別因子>
・ 血管新生阻害剤による治療歴(あり、なし)
・ 遠隔転移の初回診断からランダム化までの期間(18ヵ月以上、18ヵ月未満)
・ ECOG PS(0又は1、2)
【対象】KRAS G12C変異陽性の遠隔転移を有するCRC患者160例(日本人患者25例を含む)
【主要評価項目】無増悪生存期間(PFS)[検証的解析項目]
【副次評価項目】全生存期間(OS)、客観的奏効率[ORR、完全奏効(CR)+部分奏効(PR)]、病勢コントロール率[DCR、CR+PR+7週間以上の安定(SD)]、奏効期間(DOR)、奏効までの期間(TTR)、有害事象の発現と重症度、バイタルサインの変化、臨床検査値の変化、患者報告アウトカムの変化[簡易倦怠感調査票(BFI-SF)、簡易疼痛調査票(BPI-SF)、EORTC QLQ-C30、EuroQol-5D level5(EQ-5D-5L)、症状の煩わしさに関する単項目(FACT-G)のGP5の要約スコア、Patient Global Impression of Change(PGIC)の要約スコア]、ソトラシブ及びパニツムマブの薬物動態(PK)
【データカットオフ】2023年6月19日(OSは2023年12月18日)
〔解析計画〕
- 主要評価項目であるPFS及び重要な副次評価項目であるOSの主要解析は、最大の解析対象集団(FAS)を対象に実施した。
- PFSの主要解析は、ルマケラス960mg+パニツムマブ群と対照群でPFSイベントが約60件発生した時点で実施することとした(3群全体では約90件発生していると予測)。ルマケラス(240mg又は960mg)+パニツムマブ群と対照群に関する真の治療効果としてハザード比(HR)を0.4と仮定したとき、片側α=2.5%(両側5%)の半分である1.25%(両側2.5%)の有意水準でルマケラス+パニツムマブ群が優越性を示す検出力は90%であった。
- 事前に規定したサブグループ解析:血管新生阻害剤治療歴の有無、遠隔転移の初回診断からの期間、ECOG PS、地域、年齢、性別、人種、重複変異の有無、分化度、腫瘍占居部位、原発巣、遠隔転移診断後の治療歴(前治療数)、肝転移の有無、各薬剤使用歴(ベバシズマブ、アフリベルセプト、ラムシルマブ、免疫チェックポイント阻害剤、レゴラフェニブ、トリフルリジン/チピラシル、オキサリプラチン、イリノテカン、フッ化ピリミジン、オキサリプラチン+イリノテカン+フッ化ピリミジン)
- 日本人部分集団における有効性解析の群間比較では、各群のイベント数が極めて少ないことから、層別因子で調整しない解析も実施した。
- ルマケラス+パニツムマブ群の対照群に対するOSの優越性を検証する解析を2回実施する計画とした。PFSの主要解析の結果、ルマケラス(240mg又は960mg)+パニツムマブ群が統計学的に有意に良好であった場合、当該用量レベルでOSの中間要約を実施することとした。PFSの主要解析時には34件のOSイベントの発生が予測され、OSの真のHRが0.65の場合、本試験でHR<1となる確率は約90%であった。このOSの中間要約では、名目上の有意水準αとして0.01%を消費する想定とした(全体の第1種過誤率に及ぼす影響は無視できる)。その後、OSの最終解析は全3群において、約77件のOSイベント(約50%の成熟度)が観察された時点で実施することとした。
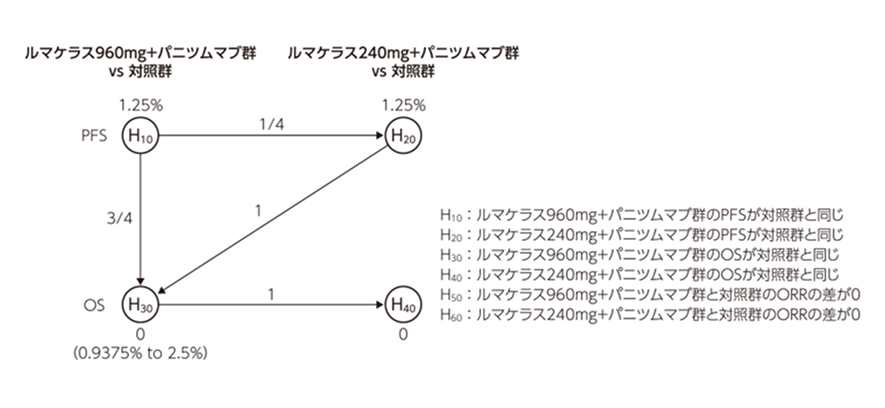
- PFS及び重要な副次評価項目(OS及びORR)に関する仮説は、試験全体の第1種過誤率を片側α=2.5%(両側α=5%)未満に制御するために、以下に示すグラフィカル多重検定法(Maurer-Bretz法)を用いて検定することとした。この方法では、1つの仮説を、他の仮説検定の棄却により再配分された新たな名目有意水準で繰り返し再検定することができる。
PFSの検定:2.5%の片側αを2つに分割し、1.25%ずつとした。H10を片側有意水準1.25%で検定し、H10が棄却された場合はH20を片側有意水準α/2+α/8(1.5625%)で検定することとした。
OSの検定:H20が棄却されればH30を片側有意水準3α/8+5α/8(2.5%)で検定し、H20が棄却されなければH30を片側有意水準3α/8(0.9375%)で検定することとした。また、H30が棄却された場合に限り、H40をH30と同じ片側有意水準で検定することとした。
ORRの検定:H30が棄却され、H20とH40がともに棄却された場合、H50を片側有意水準α(2.5%)で検定した後、H60を片側有意水準α(2.5%)で検定することとした。H30が棄却されH20が棄却されない場合(H40及びH60は検定しない)はH50を片側有意水準0.9375%で検定し、H30とH20がともに棄却されH40が棄却されない場合はすべてのαが消費され、ORRの仮説についてはいずれも検定されないこととなる。
- 副次評価項目である患者報告アウトカムの各評価項目については、投与群別及び時点別に記述的な解析を行った。また、BFI-SF、BPI-SF及びEORTC QLQ-C30については、反復測定の混合モデルを用いた解析を行い、ベースラインからの変化量の最小二乗平均値(LSM)の群間差について推定値並びに記述的なp値及び両側95%CIを算出した。
6. 用法及び用量(一部抜粋) 〈がん化学療法後に増悪したKRAS G12C変異陽性の治癒切除不能な進行・再発の結腸・直腸癌〉
パニツムマブ(遺伝子組換え)との併用において、通常、成人にはソトラシブとして960mgを1日1回経口投与する。なお、患者の状態により適宜減量する。
有効性
この試験では、主要評価項目の無増悪生存期間(PFS)についてルマケラス960mg+パニツムマブ群の対照群に対する優越性が検証されました(図12)13,14)。
-
図12 無増悪生存期間(PFS)[主要評価項目][検証的解析結果]
![図12 無増悪生存期間(PFS)[主要評価項目][検証的解析結果]](/-/media/Themes/Amgen/amgenpro-jp/amgenpro-jp/Images/Content/lumakras/combination-therapy/accordion10.png)
![図12 無増悪生存期間(PFS)[主要評価項目][検証的解析結果]](/-/media/Themes/Amgen/amgenpro-jp/amgenpro-jp/Images/Content/lumakras/combination-therapy/accordion10-sp.png)
安全性
有害事象は、ルマケラス960mg+パニツムマブ群53例(100%)、対照群49例(96.1%)で発現しました(表1)。
主な有害事象(いずれかの群で20%以上)は、低マグネシウム血症(ルマケラス960mg+パニツムマブ群34.0%、対照群2.0%、以下同順)、発疹(30.2%、2.0%)、下痢(26.4%、23.5%)、ざ瘡様皮膚炎(24.5%、2.0%)、皮膚乾燥(24.5%、2.0%)、悪心(15.1%、35.3%)、貧血(13.2%、21.6%)、嘔吐(11.3%、11.8%)、好中球減少症(0%、33.3%)でした(表1)13,14)。
-
表1 有害事象の発現状況
(データカットオフ日:2023年6月19日)
発現例数(%) ルマケラス960mg+
パニツムマブ群
(n=53)ルマケラス240mg+
パニツムマブ群
(n=53)対照群
(n=51)有害事象 53(100) 53(100) 49(96.1) 主な事象(いずれかの群で20%以上) 低マグネシウム血症 18(34.0) 18(34.0) 1(2.0) 発疹 16(30.2) 12(22.6) 1(2.0) 下痢 14(26.4) 14(26.4) 12(23.5) ざ瘡様皮膚炎 13(24.5) 22(41.5) 1(2.0) 皮膚乾燥 13(24.5) 14(26.4) 1(2.0) 悪心 8(15.1) 16(30.2) 18(35.3) 貧血 7(13.2) 8(15.1) 11(21.6) 嘔吐 6(11.3) 12(22.6) 6(11.8) 好中球減少症 0 0(0) 17(33.3) 重篤な有害事象 14(26.4) 17(32.1) 15(29.4) 主な事象(いずれかの群で3例以上) 敗血症 3(5.7) 0 0 腸閉塞 2(3.8) 3(5.7) 0 小腸閉塞 0 3(5.7) 0 減量に至った有害事象 11(20.8) 10(18.9) 11(21.6) 投与中断に至った有害事象 26(49.1) 32(60.4) 29(56.9) 投与中止に至った有害事象* 1(1.9) 3(5.7) 2(3.9) 死亡に至った有害事象 2(3.8) 4(7.5) 3(5.9) 心停止(1例) 腸閉塞(2例) 急性心不全(1例) 敗血症(1例) 中枢神経系転移(1例) 状態悪化(1例) 腹膜転移(1例) 胸膜痛(1例) *:【事象名】ルマケラス960mg+パニツムマブ群は低カルシウム血症(1例)、ルマケラス240mg+パニツムマブ群は腹膜転移、悪心(各1例)、対照群は呼吸困難、胸膜痛、肝不全(各1例)でした。また、ルマケラス240mg+パニツムマブ群の1例は小腸閉塞によりルマケラスのみを中止しました。
※対照群に割り付けられながら治験薬を投与されなかった3例は、安全性解析対象集団に含めていません。
6. 用法及び用量(一部抜粋) 〈がん化学療法後に増悪したKRAS G12C変異陽性の治癒切除不能な進行・再発の結腸・直腸癌〉
パニツムマブ(遺伝子組換え)との併用において、通常、成人にはソトラシブとして960mgを1日1回経口投与する。なお、患者の状態により適宜減量する。
-
References
- Tanaka N, Ebi H. Cancer Sci. 2025; 116: 600-612. [利益相反:著者にAmgen社から資金提供を受けた者を含む]
- Chida K, et al. Oncologist. 2021; 26: 845-853. [利益相反:著者にAmgen社から資金提供を受けた者を含む]
- Muñoz-Maldonado C, et al. Front Oncol. 2019; 9: 1088.(SOT00145)
- Takács T, et al. Cancer Metastasis Rev. 2020; 39: 1051-1065.(SOT00146)
- Cox AD, et al. Nat Rev Drug Discov. 2014; 13(11): 828-851.(SOT00008)
- Ostrem JM, et al. Nature. 2013; 503: 548-551.(SOTQ00166)
- Canon J, et al. Nature. 2019; 575: 217-223.(SOT00025) [利益相反:本試験はアムジェン社の支援により行われた。]
- Hong DS, et al. N Engl J Med. 2020; 383: 1207-1217.(SOT00030) [利益相反:本試験はアムジェン社の支援により行われた。]
- Corcoran RB, et al. Cancer Discov. 2012; 2: 227–235.
- Amodio V, et al. Cancer Discov. 2020; 10: 1129–1139. [利益相反:著者にAmgen社から資金提供を受けた者を含む]
- 日本臨床腫瘍学会 編. 大腸がん診療における遺伝子関連検査等のガイダンス 第5版. 2023年3月. 金原出版. P10-21, 91-94, 2023.
- 大腸癌研究会 編. 大腸癌 治療ガイドライン 医師用 2024年版. 37-53, 金原出版, 2024.
- 社内資料:20190172試験 国際共同第Ⅲ相試験 [承認時評価資料]
- Fakih MG, et al. N Engl J Med. 2023; 389(23): 2125-2139. [利益相反:本試験はアムジェン社の支援により行われた。]







